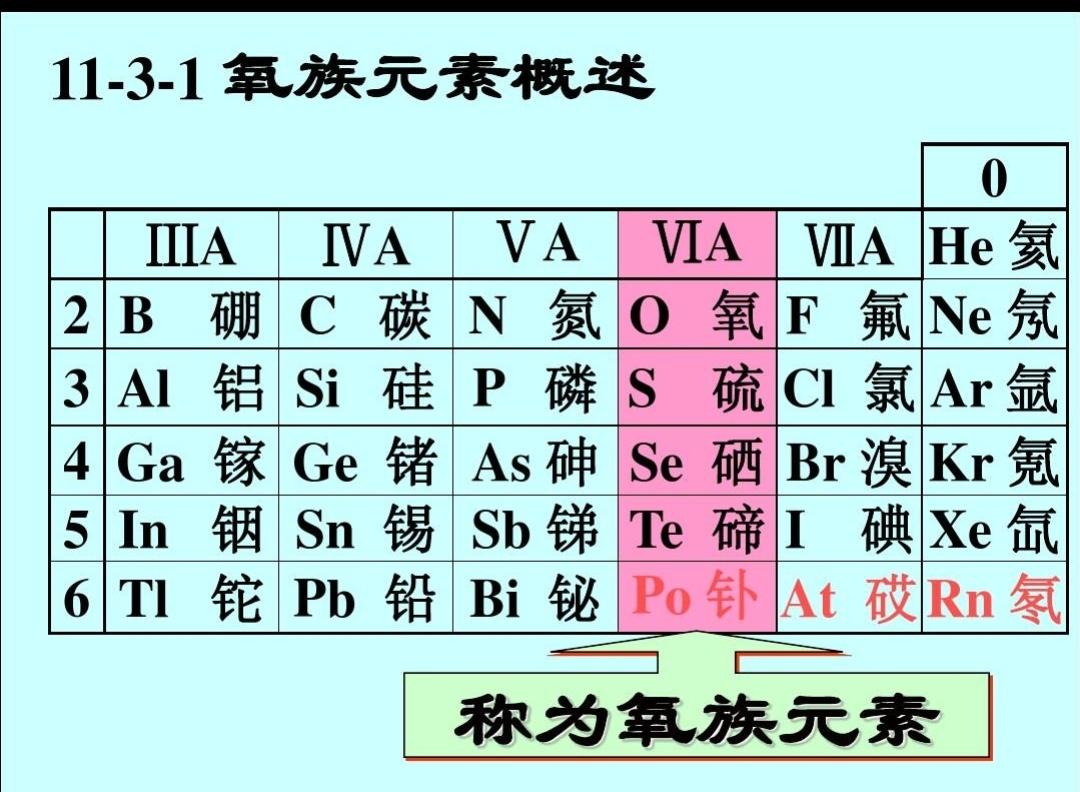
硫(氧族元素)
温馨提示:这篇文章已超过417天没有更新,请注意相关的内容是否还可用!

硫
氧族元素
硫是一种化学元素,在元素周期表中它的化学符号是S,原子序数是16。是一种非常常见的无味无嗅的非金属,纯的硫是黄色的晶体,又称做硫磺。硫有许多不同的化合价,常见的有-2, 0, +4, +6等(在二硫化铁中硫显-1)。在自然界中它经常以硫化物或硫酸盐的形式出现,尤其在火山地区纯的硫也在自然界出现。对所有的生物来说,硫都是一种重要的必不可少的元素,它是多种氨基酸的组成部分,由此是大多数蛋白质的组成部分。它主要被用在肥料中,也广泛地被用在火药、润滑剂、杀虫剂和抗真菌剂中。
| 中文名 | 硫 |
| 外文名 | sulfur |
| 别名 | 硫磺 硫黄 |
| 熔点 | 112.8 |
| 沸点 | -60.70 |
| 水溶性 | 难溶于水 |
| 密度 | 2.36 |
| 外观 | 淡黄色晶体 |
| 闪点 | 168 |
| 应用 | 农业,医药,橡胶,建材,火药,火柴,酿酒,制糖等领域 |
| 安全性描述 | S16;S26 |
| 危险性符号 | R11 |
| 危险性描述 | F |
| UN危险货物编号 | 2448/1350 |
| 符号 | S |
| 序号 | 16 |
| 族 | 氧族(VIA族) |
| 周期 | 3 |
| 元素分区 | p |
| 原子质量 | 32.065 原子量单位 |
简介

硫,是一种淡黄色晶体。有单质硫和化合态硫两种形态。
单质硫有几种同素异形体:
主要是菱形硫(S8),密度2.07克/厘米 ,熔点112.8℃,沸点444.674℃;单斜硫(S8),密度1.96克/厘米3,熔点119.0℃,沸点444.6℃;纯粹的单质硫,密度1.96克/厘米3,熔点120.0℃,沸点444.6℃。导热性和导电性都差。性松脆,不溶于水。
无定形硫主要有弹性硫,是由熔态硫迅速倾倒在冰水中所得。不稳定,可转变为晶状硫。晶状硫能溶于有机溶剂如二硫化碳中,而弹性硫只能部分溶解。化合价为-2、+2、+4和+6。第一电离能10.360电子伏特。
亚洲最大的硫磺生产基地,世界上最大的3座天然气脱硫厂在达州。
发现历史
硫在远古时代就被人们所知晓。大约在4000年前,埃及人已经会用硫燃烧所形成的二氧化硫来漂白布匹,古希腊和古罗马人也能熟练地使用二氧化硫来熏蒸消毒和漂白。公元前九世纪,古罗马著名诗人荷马在他的著作里讲述了硫燃烧时有消毒和漂白的作用。
硫在古代中国被列为重要的药材,在中国古代第一部药物学专著《神农本草经》中所记载的46种矿物药品中,就有石硫黄(即硫磺)。在这部著作里还指出:“石硫黄能化金银铜铁,奇物”。这说明当时已经知晓硫能与铜、铁等金属直接作用而生成金属硫化物。世界现存最古的炼丹著作——魏伯阳的《周易参同契》,也记述了硫能和易挥发的汞化合成不易挥发的硫化汞。在东晋炼丹家葛洪的《抱朴子内篇》中也有“丹砂烧之成水银,积变又还成丹砂”的记载。中国对火药的研究,大概始于公元七世纪。当时的火药是黑火药,它是由硝酸钾、硫黄和木炭三者组成。火药的制造促进了硫磺的提取和精制技术的发展,《太清石壁记》有用升华法精制硫磺的记载。明朝末年宋应星的《天工开物》一书中对从黄铁矿石和含煤黄铁矿石制取硫磺的操作方法作了详细的叙述。
随着1746年英国J.Roebuck发明了铅室法制造硫酸和1777年硫被法国 A.L.Lavoisier确认为一种元素后,硫便进入了近代化学的大门。在此之后的年代,硫就迅速成为与近代化学工业和现代化学工业密切相关的最重要的元素之一。
含量分布
硫在自然界中分布较广,在地壳中含量为0.048%(按质量计)。在自然界中硫的存在形式有游离态和化合态。单质硫主要存在于火山周围的地域中。以化合态存在的硫多为矿物,可分为硫化物矿和硫酸盐矿。硫化物矿有黄铁矿(FeS2)、黄铜矿(CuFeS2)、方铅矿(PbS)、闪锌矿(ZnS)等。硫酸盐矿有石膏(CaSO4·2H2O)、芒硝(Na2SO4·10H2O)、重晶石(BaSO4)、天青石(SrSO4)、矾石[(AlO)2SO4·9H2O]、明矾石[K2SO4·Al2(SO4)3·24H2O]等。
物理性质
 硫
硫硫有25种同位素,其中四种是稳定的:S-32(95.02%)、S-33(0.75%)、S-34(4.21%)和S-35(0.02%),除35S外,其它放射性同位素的半衰期都很短。硫-35由宇宙射线射击空气中的氩-40而导致,其半衰期为87.48年。
硫化物沉淀时根据温度的不同S-34的含量少许不同。假如在一个矿物中硫化物和碳酸盐同时存在的话,那麼根据碳-13和硫-34的含量可以推算出矿物形成时矿水的pH值和氧的逸度。
在森林生态系统中,硫酸盐主要来自空气,少量来自矿物的风化。其中硫的同位素的不同含量可用来确定它们的来历。
原子半径:102pm;
离子半径:184pm(S2-),29pm(S4+);
纯的硫呈浅黄色,质地柔软、轻,粉末有臭味。硫不溶于水但溶于二硫化碳。硫在所有的物态中(固态、液态和气态),硫都有不同的同素异形体,这些同素异形体的相互关系还没有被完全理解。晶体的硫可以组成一个由八个原子组成的环:S8。
导热性和导电性都差。性松脆,不溶于水。无定形硫主要有弹性硫,是由熔态硫迅速倾倒在冰水中所得。不稳定,可转变为晶状硫。晶状硫能溶于有机溶剂如二硫化碳(而弹性硫只能部分溶解)、四氯化碳和苯。化合价为-2.+2.+4和+6。第一电离能10.360电子伏特。结晶形硫不溶于水,稍溶于乙醇和乙醚,溶于二硫化碳、四氯化碳和苯。可转变为晶状硫(正交硫),正交硫是室温下唯一稳定的硫的存在形式。原子半径:88pm。
化学性质
化合价为-2、+2、+4和+6。第一电离能10.360电子伏特。化学性质比较活泼,能与氧、金属、氢气、卤素(除碘外)及已知的大多数元素化合。还可以与强氧化性的酸、盐、氧化物,浓的强碱溶液反应。它存在正氧化态,也存在负氧化态,可形成离子化合物、共价化合成物和配位共价化合物。
1、氧化性
与金属单质反应:铜→硫化亚铜;铁→硫化亚铁;铝,钠等金属往往将其氧化为较底价态 特性:银与硫摩擦生成硫化银;汞与硫研磨生成硫化汞,实验室水银温度计打破流出水银时,撒上硫粉可防止汞蒸气生成。
与非金属反应:2S+C→CS2;S+H2→H2S
与其他的还原剂:S+Na2SO3加热→Na2SO3S(Na2S2O3)
2、还原性: S+O2 点燃→SO2
硫在氧气里燃烧的现象:剧烈燃烧,发出热量,发出明亮的蓝紫色火焰,生成有刺激性气味的气体。硫与氧气燃烧会生成二氧化硫。
3、既氧化又还原:
3S+6KOH加热→2K2S+K2SO3+2H2O (歧化反应)
4、常见化学方程式
(x+3)S + 6 OH- =加热=2S(x/2+1) + SO3 + 3H2O
3S + 2Al + 6H2O ==== 2Al(OH)3↓ +3H2S↑
S +2Fe ==== 2Fe +S↓
S2O3 +2H ==== S↓ + SO2↑ + H2O
2H2S + SO2=(点燃)=== 3S↓+ 2H2O
2H2S +O2==== 2S↓+2H2O(点燃,氧气不足)
制取方法
1.往二氧化硫中通入氢硫酸,可以制取硫。化学方程式:SO2+2H2S=3S↓+2H2O(氧化还原反应)
2.往酸性高锰酸钾中通入氢硫酸。化学方程式:2KMnO4+ 5H2S+3H2SO4=K2SO4+2MnSO4+ 5S↓+ 8H2O
3.往亚硫酸中通入硫化氢。化学方程式:11.2H2S+H2SO3=3S↓+3H2O
化合物
许多有机物难闻的味道来自于它们所含有硫化氢之类的化合物。这些化合物有一股特别的臭鸡蛋味道。
硫化氢的溶液是酸性的,与金属反应形成金属的硫化物。铁的硫化物在大自然中很常见,被称为黄铁矿。方铅矿是硫化铅,也是第一种被发现的半导体。
 硫
硫聚合的氮化硫有金属特性,尽管它不含任何金属,这个复合物还显示特别的电学和光学特性。让熔化的硫速凝可以获得无晶态的硫,伦琴衍射显示其中含有由八个硫原子组成的环。这种硫在室温下不十分稳定,它渐渐恢复为晶体状态。
其它重要的硫的化合物
连二亚硫酸钠:Na2S2O4,是一种强有力的还原剂
亚硫酸:H2SO3,是二氧化硫在水中的溶液。亚硫酸和亚硫酸盐是有力的还原剂。二氧化硫的其它产物包括焦亚硫酸离子(S2O5 )
硫代硫酸物:S2O3 ,是氧化物。硫代硫酸氨有可能可以代替氰化物来洗金
连二硫酸:H2S2O6,及其盐
连多硫酸:H2SnO6,n可以从3一直到80
硫酸盐:是硫酸的盐
硫化物:是硫与其它元素的化合物
过一硫酸是三氧化硫与浓的过氧化氢的反应物
硫氰酸盐是硫氰离子(SCN )的化合物
硫氰:(SCN)2
二硫化碳
同位素
硫有18种同位素,其中四种是稳定的:S-32(95.02%)、S-33(0.75%)、S-34(4.21%)和S-36(0.02%),除 S外,其它放射性同位素的半衰期都很短。硫-35由宇宙射线射击空气中的氩-40而导致,其半衰期为87天。
硫化物沉淀时根据温度的不同S-34的含量少许不同。假如在一个矿物中硫化物和碳酸盐同时存在的话,那么根据碳-13和硫-34的含量可以推算出矿物形成时矿水的pH值和氧的逸度。
在森林生态系统中,硫酸盐主要来自空气,少量来自矿物的风化。其中硫的同位素的不同含量可用来确定它们的来历。
硫单质及其化合物
(一)硫单质的反应(非金属性弱于卤素、氧和氮)
1.硫与氧气反应(只生成二氧化硫,不生成三氧化硫)
2.硫与氢气加热反应
3.硫与铜反应(生成+1价铜化合物,即硫化亚铜)
4.硫与铁反应,(生成+2价铁化合物,即硫化亚铁)
 硫
硫5.硫与汞常温反应,生成HgS(撒落后无法收集的汞珠应撒上硫粉,防止汞蒸气中毒)
7.硫与强碱溶液反应生成硫化物和亚硫酸盐(试管上粘附的硫除了可用CS2洗涤以外,还可以
用NaOH溶液来洗)3S+6NaOH=2Na2S+Na2SO3+3H2O
(二)二氧化硫或亚硫酸的反应(弱氧化性,强还原性,酸性氧化物)
1.氧化硫化氢
2.被氧气氧化(工业制硫酸时用催化剂;空气中的二氧化硫在某些悬浮尘埃和阳光作用下被氧气氧化成三氧化硫,并溶解于雨雪中成为酸性降水。)
3被卤素氧化SO2+Cl2+2H2O==H2SO4+2HCl
4.与水反应
5.与碱性氧化物反应
6.与碱反应
7.有漂白性(与有机色质化合成无色物质,生成的无色物质不太稳定,受热或时日一久便返色)
(三)硫酸性质用途小结
1.强酸性
(1)、与碱反应
(2)、与碱性氧化物反应(除锈;制硫酸铜等盐)
(3)、与弱酸盐反应(制某些弱酸或酸式盐)
(4)、与活泼金属反应(制氢气)
2.浓硫酸的吸水性(作气体干燥剂;)
3.浓硫酸的脱水性(使木条、纸片、蔗糖等炭化;乙醇脱水制乙烯)
4.浓硫酸的强氧化性
(1)、使铁、铝等金属钝化;
(2)、与不活泼金属铜反应(加热)
(3)、与木炭反应(加热)
(4)、制乙烯时使反应混合液变黑
5.高沸点(不挥发性)(制挥发性酸)
(1)、制氯化氢气体
(2)、制硝酸(HNO3易溶,用浓硫酸)
实验室制二氧化碳一般不用硫酸,因另一反应物通常用块状石灰石,反应生成的硫酸钙溶解度
小易裹在表面阻碍反应的进一步进行。
6.有机反应中常用作催化剂
(1)、乙醇脱水制乙烯(作催化剂兼作脱水剂,用多量浓硫酸,乙醇浓硫酸体积比1∶3)
(2)、苯的硝化反应(硫酸作催化剂也起吸水作用,用浓硫酸)
(3)、酯化反应(硫酸作催化剂和吸水剂,用浓硫酸)
(4)、酯水解(硫酸作催化剂,用稀硫酸)
(5)、糖水解(注意:检验水解产物时,要先加碱中和硫酸)
主要用途
工业需求
硫在工业中很重要,比如作为电池中或溶液中的硫酸;硫被用来制造火药;在橡胶工业中做硫化剂。硫还被用来杀真菌、用做化肥。硫化物在造纸业中用来漂白。硫酸盐在烟火中也有用途。硫代硫酸钠和硫代硫酸氨在照相中做定影剂。制造硫酸、亚硫酸盐、杀虫剂、塑料、搪瓷、合成染料、橡胶硫化、漂白、药物、油漆。
硫矿物最主要的用途是生产硫酸和硫磺。硫酸是耗硫大户,中国约有70%以上的硫用于硫酸生产。化肥是消费硫酸的最大户,消费量占硫酸总量的70%以上,尤其是磷肥耗硫酸最多,增幅也最大。硫酸除用于化学肥料外,还用于制作苯酚、硫酸钾等90多种化工产品;轻工系统的自行车、皮革行业;纺织系统的粘胶、纤维、维尼纶等产品;冶金系统的钢材酸洗、氟盐生产部门;石油系统的原油加工、石油催化剂、添加剂以及医药工业等都离不开硫酸。随着中国经济的发展,各行业对硫酸的需求量均呈缓慢上升趋势,化肥用项是明显的增长点。
高品位硫铁矿烧渣可以回收铁等;低品位的烧渣可作水泥配料。烧渣还可以回收少量的银、金、铜、铝、锌和钴等。硫磺除为生产硫酸的原料之外,还广泛用来生产化工产品,如硫化铜、焦亚硫酸钠等。另外,在食糖生产中,要把硫磺氧化为二氧化硫气体用于漂白脱色。在农药生产中也直接或间接使用硫磺;粘胶纤维生产中需用二硫化碳作溶剂;硫化金属矿浮选用的药剂要以二硫化碳为原料;除以上应用外,消费硫磺的行业还有火柴制造、水泥枕轨处理、医药、火药等。
比如作为电池中或溶液中的硫酸。硫被用来制造火药。硫也是生产橡胶制品的重要原料。硫还被用来杀真菌,用做化肥。硫化物在造纸业中用来漂白。硫还可用于制造黑色火药、焰火、火柴等。硫代硫酸钠和硫代硫酸氨在照相中做定影剂。硫又是制造某些农药(如石灰硫黄合剂)的原料。
生理作用
半胱氨酸、蛋氨酸、同型半胱氨酸和牛磺酸等氨基酸和一些常见的酶含硫,因此硫是所有细胞中必不可少的一种元素。在蛋白质中,多肽之间的二硫键是蛋白质构造中的重要组成部分。有些细菌在一些类似光合作用的过程中使用硫化氢作为电子提供物(一般植物使用水来做这个作用)。植物以硫酸盐的形式吸收硫。无机的硫是铁硫蛋白的一个组成部分。在细胞色素氧化酶中,硫是一个关键的组成部分。
医疗上,硫还可用来制硫黄软膏医治某些皮肤病,但硫对身体危害较大长期在高含硫的工况下工工作对身体有极大损害。
危险性
工业硫磺为易燃固体。此外,空气中含有一定浓度硫磺粉尘时不仅遇火会发生爆炸,而且硫磺粉尘也很易带静电产生火花导致爆炸(硫磺粉尘爆炸下限为2.39/m),继而燃烧引发火灾。按固体火灾危险性分类硫磺属于乙类,硫磺回收和成型装置属于火灾危险性乙类装置。人体吸入硫磺粉尘后还会引起咳嗽、喉痛等。
燃烧爆炸危险性
①正常情况下燃烧缓慢,与氧化剂混合时燃烧速度剧增;②与氧化剂混合可形成爆炸性混合物;③遇明火、高温易发生火灾;④粉尘易带高达数千伏乃至上万伏静电;⑤摩擦产生的高温和明火等均可导致硫磺粉尘爆炸和火灾;⑥一般情况下硫磺粉尘比易燃气体更易发生爆炸,但燃烧速度和爆炸压力比易燃气体小。
毒性
接触限值:中国MAC、美国TWA和STEL均未制定标准 毒理资料:低毒性。
对人体危害
①因其可在肠内部分转化为硫化氡而被人体吸收,故大量吞入(10~209)可导致硫化氢中毒;
②可引起眼结膜炎、皮肤湿疹,对皮肤有弱刺激性;
③长期吸入硫磺粉尘一般无明显毒性。
防御措施
根据国家标准《工业硫磺》(GB 2449—2006)规定,有关工业硫磺安全等防护事项如下。
(1) 安全
从事工业硫磺生产、运输、储存及加工的工作人员,操作时应使用必要的防护用品。
严格遵守国家有关消防、危险品的安全条例。工业硫磺堆放场所和仓库应设置专门灭火器材,严禁明火。允许以喷水等方法熄灭烧着的硫磺。
由于硫磺粉尘易爆,使用和运输工业硫磺时应防止生成或泄出硫磺粉尘。液体硫磺的生产、储运以及使用遵照相关安全规定执行。
(2) 标志、包装、运输和储存
工业硫磺的包装容器上应有明显、牢固的标志,内容包括生产厂名、厂址、产品名称、商标、等级、净质量、批号、生产日期、《工业硫磺》标准编号和符合GB 190规定的“易燃固体”标志。
固体产品可用塑料编织袋或内衬塑料薄膜袋包装,也可散装。其中,包装块状硫磺可不用内衬塑料薄膜袋,散装产品应遮盖,但粉状硫磺不可散装。液体硫磺应使用专门容器储装。
(3)产品的运输按国家有关规定行
块状、粒状硫磺可储存于露天或仓库内。粉状、片状硫磺储存于有顶盖的场所或仓库内。
袋装产品成垛堆放,堆垛间应留有不少于0.75m宽的通道。不许放置在上下水管道和取暖设备的近旁。
代表案例
(1) 硫磺仓库爆炸事故
2008年1月13日,国内某公司的一个分公司硫磺仓库发生爆炸,造成7人死亡、32人受伤。
① 事故经过 2008年1月13日2时45分,铁路运输装卸承包单位的53名工人在该公司硫磺仓库内开始从事火车硫磺卸车作业,即从火车卸下并拆开硫磺包装袋,将硫磺分别倒入平行于铁路、与地面平齐的34个料斗中,硫磺通过料斗落在地坑中输送机皮带上,用输送机传送皮带将硫磺送入硫磺库内作为该公司生产硫酸的原料。3时40分时地坑硫磺粉尘突然发生爆炸,爆炸冲击波将料斗、硫磺库的轻型屋顶、皮带输送机、斗式提升机等设备、设施毁坏,造成7人死亡、7人重伤、25人轻伤。
② 事故原因事故发生的主要原因,一是天气干燥,空气湿度低,硫磺粉尘容易爆炸;二是作业时正值深夜,风速低,空气流动性差,造成局部空间内(皮带运输机地坑)硫磺粉尘浓度增大,达到爆炸极限,由现场产生的点火能量引发爆炸。
(2) 硫磺成型系统爆炸事故
国内某厂有两套硫磺回收装置,共用一台成型结片机,生产能力7500t/a。成型系统包括成型结片机(二楼)、包装间和成品库(一楼),包装间和成品库混用。
2001年6月23日14时10分,一搬运工将无防火帽的外运货车开进硫磺成品库,引起成品库内小范围闪爆,幸无人员伤亡。
2003年1月19日10时30分,一电工在拆修成型结片机顶部引风线上的轴流风机时,产生的电火花造成引风线内硫磺粉尘爆炸,爆炸产生的冲击波将现场一名作业人员推出1.5m远,所幸有护栏保护,未造成伤亡。
参考资料
1.60秒,认识中国达州·腾讯网
2.·
3.工业硫磺危险性与防护· 安全管理网